


Тонзиллэктомия для большинства пациентов с хроническим декомпенсированным тонзиллитом является методом выбора и зачастую единственным способом лечения. В связи с этим тонзиллэктомия — одна из наиболее рас-пространенных плановых операций в ЛОР-хирургической практике. Этот метод хирургического лечения, по данным разных авторов, достигает до 40% от всех хирургических вмешательств на ЛОР-органах [1—3]. Показаниями для хирургического вмешательства являются частые ангины, а также местные осложнения ангин, такие как паратонзиллярный абсцесс, заглоточный абсцесс, флегмона шеи, на-гноившийся шейный лимфаденит, фебрильные судороги, выраженная тонзиллогенная интоксикация, заболевания отдаленных органов и систем, связанные с патологией глот-ки [4]. В послеоперационном периоде после тонзиллэктомии боль остается чрезвычайно актуальным и в большинстве случаев единственным симптомом. Причинами боли непосредственно после тонзиллэктомии и в ближайшие не-сколько дней являются обширная открытая послеоперационная поверхность в тонзиллярных нишах, отек и инфильтрация небных дужек [5]. Механизм посттравматической боли связан с повышением возбудимости ноцицепторов, возникающим в результате действия альгогенов — веществ, выделяющихся из поврежденных в результате хирургического воздействия клеток (гистамин, серотонин, АТФ, лейкотриены, интерлейкин-1, фактор некроза опухоли, эндотелины, простагландины, оксид азота, нейрокинин А и др.) и образующихся в плазме крови (брадикинин). Наиболее часто после операции пациентов беспокоит выраженная боль в горле, которая зачастую иррадиирует в уши, а также усиливается при глотании [6]. В этих случаях необходимо прибегать к помощи обезболивающих препаратов, а также соблюдать специальную диету, исключающую грубую, соленую, пряную пищу. Послеоперационная боль негативно влияет на приемы пищи и возвращение к активной повседневной жизни пациента.
Кроме того, возникает опасность микробной контаминации раневой поверхности на фоне снижения местного иммунитета и противоинфекционной резистентности воспаленных тканей. В связи с этим важной проблемой после тонзиллэктомии являются уменьшение явлений реактивного воспаления тканей, уменьшение болевого синдрома, возникающего в ответ на операционную травму.
Для достижения оптимального обезболивающего эффекта после тонзиллэктомии требуется применение большого количества различных анальгетических препаратов.
По данным литературы, за годы проведения тонзиллэктомии проводились множественные попытки совершенствования обезболивания в послеоперационном периоде, как системными препаратами, так и местными. Однако многие из них обладают побочными эффектами и плохо применимы в современной практике.
Применение опиоидов имеет такие побочные эффекты, как тошнота, рвота, запор, угнетение дыхания и сильная седация.
Нестероидные противовоспалительные препараты (НПВП) повышают риски кровотечений и желудочно-кишечных расстройств. По мнению экспертов, ибупрофен обладает некоторыми преимуществами в отношении переносимости перед другими нестероидными противовоспалительными препаратами [7]. Ингибиторы циклооксиге-назы-2 (целекоксиб) обладают такими же анальгезирующими свойствами, как и неселективные НПВП, и имеют минимальные побочные эффекты, такие как дисфункция тромбоцитов и желудочно-кишечные кровотечения. Однако одно из исследований показало, что целекоксиб не обеспечивает достаточный анальгетический эффект после тонзиллэктомии, а также зачастую вызывает рвоту [8].
H. Tolska и соавт. [9] провели метаанализ 29 исследований, представляющих двойное слепое плацебо-контролируемое рандомизированное исследование системных анальгетиков, применяющихся в послеоперационном периоде после тонзиллэктомии. Это исследование подтвердило полезные анальгетические эффекты парацетамола, НПВП, дексаметазона, габапентиноидов и декстрометорфана после тонзиллэктомии в день операции. Дексаметазон в многократных дозах имел обезболивающий эффект, превышающий 24 ч. Тем не менее использование стероидов с высокими суммарными дозами и/или длительный прием после операции должны осуществляться с осторожностью, принимая во внимание возможные риски. Хорошо известные побочные эффекты системной глюкокортикостероидной терапии (например, лунообразное лицо, синдром Ку-шинга, сахарный диабет) развиваются при долгосрочном лечении. Риск развития побочных эффектов от краткосрочной, в течение 1—2 нед, системной глюкокортикостероидной терапии минимален, если лечение не проводится пациентам с диабетом, глаукомой, катарактой и остеопорозом. Однако повышение уровня глюкозы крови и подъем артериального давления могут наблюдаться на фоне лечения системными глюкокортикостероидами и у пациентов без сахарного диабета, гипертонической болезни. Одно-кратный прием анальгетиков или применение только дексаметазона не обеспечивают клинически значимого дли-тельного анальгетического эффекта после тонзиллэктомии.
A. Khan и соавт. обнаружили, что габапентин, прегабалин и декстрометорфан могут быть полезны в умеренных дозах в качестве адъювантов для других анальгетиков. Однако габапентин и прегабалин относятся к противоэпилептическим средствам, декстрометорфан — к противокашлевым, в связи с чем само обезболивающее их действие не оправ-дано. Для обезболивания после операции может быть использован кетамин — NMDA-антагонист, применяемый в качестве средства для наркоза. Его использование в субанестетических дозах эффективно при различных типах опе-раций для снижения потребности в опиоидах и болевой чувствительности. Однако пациент, получающий кетамин, дол-жен находиться под постоянным контролем врача [10].
Таким образом, системные анальгетические препараты не всегда имеют хороший обезболивающий эффект и в большинстве случаев имеют побочные эффекты. В связи с этим, чтобы избежать системного действия НПВП и при этом обеспечить непосредственный контакт лекарственного средства со слизистой оболочкой полости рта и глотки, необходимо было разработать препараты местного обезболивающего действия.
Топические препараты, используемые в комплексной терапии патологических состояний полости рта и глотки, условно можно разделить на анальгетики, противовоспалительные средства, антисептики, препараты с противоотечным действием на слизистую оболочку и т.д. [11]. Препараты местного действия в виде таблеток для рассасывания, спреев, растворов для полосканий стали также применяться у пациентов после тонзиллэктомии.
Многие исследования, проведенные у взрослых пациентов после тонзиллэктомии, показали терапевтическую эффективность бензидамина, особенно при применении 0,15% раствора для полоскания рта или спрея — отмечалось быстрое купирование болевого синдрома в горле, рефлекторной оталгии, отсутствие вторичных бактериальных осложнений. Однако в этих исследованиях есть упоминания о таком неприятном ощущении у некоторых пациентов, как жжение в глотке, связанное с входящим в состав этих препаратов этиловым спиртом. Это может указывать на раздражающий эффект данных препаратов, а также на риск возникновения кровотечений из миндаликовых ниш [12, 13]. Местная терапия для ротоглотки может включать в себя полоскание, применение спрея и рассасывания лекарственных средств. Полоскание лекарственными препаратами эффективно в отношении лечения ротовой поло-сти и основания корня языка. Применение спрея позволяет орошать заднюю стенку глотки, однако использование распылителей не рекомендовано детям в возрасте до 6 лет и у больных бронхиальной астмой. При оценке эффективности лекарственных препаратов в форме рассасывания отмечено, что концентрация активных ингредиентов в слизистой оболочке глотки более высокая, чем при применении спрея и полоскания. А также наблюдается более мед-ленное очищение слизистой оболочки глотки от лекарственных препаратов при применении лекарств в форме для рассасывания, что обеспечивает поддержание высокой концентрации препарата в очаге воспаления [14].
В поисках немедикаментозной аналгезии применяются различные виды нетрадиционных подходов к обезболиванию. Одним из таких подходов является транскраниальная электростимуляция. Установлено, что под влиянием этого метода снижается чувствительность периферических болевых рецепторов. Этот эффект вызывается увеличен-ной концентрацией циркулирующего в крови β-эндорфина. Однако этот метод имеет ряд противопоказаний и снижает выраженность боли на ограниченный период времени, а также он экономически невыгодный [15].
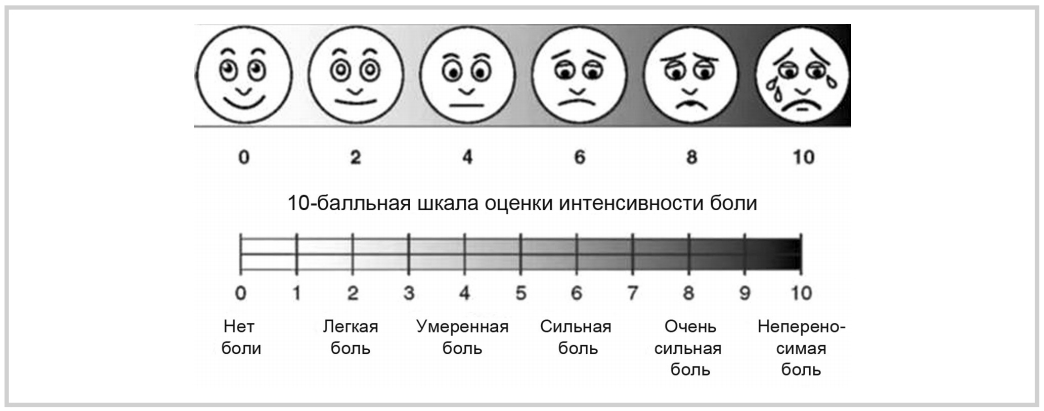
Применение визуальной аналоговой шкалы (ВАШ) для оценки боли позволяет оценить уровень острого после-операционного болевого синдрома у пациентов, перенесших тонзиллэктомию [16].
В связи с проблемой обезболивания пациентов в послеоперационном периоде после перенесенной тонзиллэктомии в последние годы осуществляются попытки производства новых безопасных современных препаратов. Од-ним из таких препаратов является Арника Монтана С9 (БУАРОН) — гомеопатический монокомпонентный препарат растительного происхождения.
Цель исследования — выявить влияние гомеопатического монокомпонентного препарата растительного происхождения Арника Монтана С9 (БУАРОН) на состояние пациентов, перенесших тонзиллэктомию.
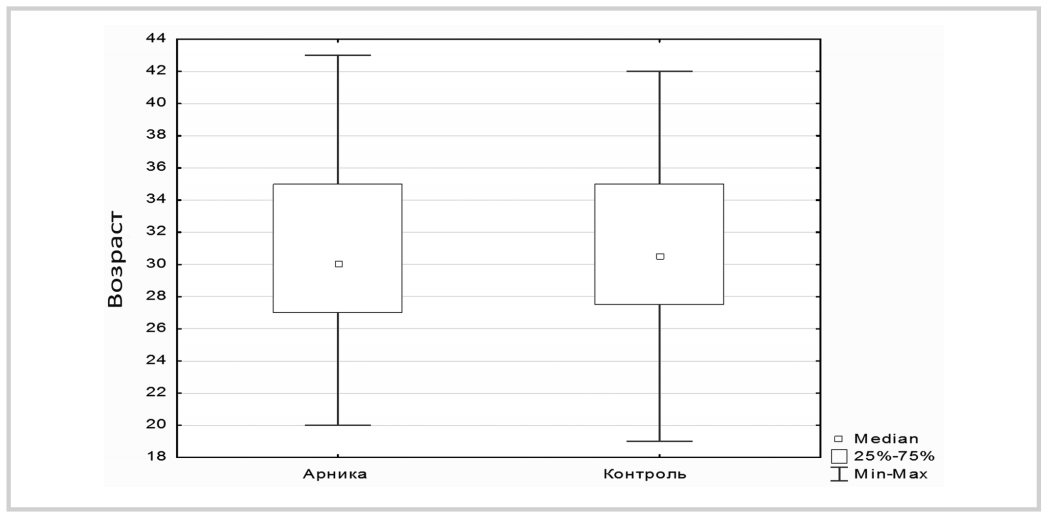
Исследование проводилось у пациентов с хроническим декомпенсированным тонзиллитом, поступивших на кафедру оториноларингологии ПСПбГМУ им. акад. И.П. Павлова для планового оперативного лечения. В 1-ю группу вошли 23 пациента в возрасте от 20 до 43 лет, которые в послеоперационном периоде получали НПВП (Кеторолак) по требованию при болях, а также гомеопатический монокомпонентный препарат растительного происхождения Арника Монтана С9 (БУАРОН) по 5 гранул 3 раза в день для рассасывания со 2-го дня. Во вторую (контрольную) группу пациентов были включены 20 пациентов в возрасте от 19 до 42 лет, получавшие только терапию НПВП по требованию (рис. 1). Две исследуемые группы пациентов были сбалансированы по полу и возрасту, та-ким образом, исследуемые различия между ними отражают эффект препарата Арника Монтана С9 (БУАРОН). Всем пациентам выполнялась классическая двусторонняя тонзиллэктомия в условиях общей анестезии одной операционной бригадой. В раннем послеоперационном периоде у всех пациентов оценивали ряд критериев: темпе-ратура тела утром после пробуждения и вечером, необходимость применения НПВП, количество их применения в сутки, оценка боли по ВАШ, а также изменения в фарингоскопической картине и лимфаденопатия шеи в течение 10 дней после операции.


Результаты в ходе проведенного исследования вносились в разработанную компьютерную базу данных на персональном компьютере при помощи таблиц Microsoft Excel. С помощью пакета прикладных программ Statistica for Windows v.10.0 проведены анализ и статистическая обработка полученных данных, определялись параметры описатель-ной статистики.
Количественные показатели были проверены на соответствие нормальному распределению с помощью критерия Колмогорова—Смирнова. Для количественных данных, имеющих нормальное распределение, были рассчитаны среднее арифметическое (М) и стандартное отклонение (SD), которые представлены в формате М (SD); при описании показателей, отличающихся от нормального распре-деления, в формате Me (Q1; Q3) использовались медианы (Me) и в качестве интервальной оценки — нижний Q1 (25%) и верхний Q3 (75%) квартили. Качественные показатели исследования представлены в абсолютных и относительных величинах (%).
Для нахождения различий между нормально распре-деленными показателями использовался t-критерий Стьюдента.
Формула t-критерий Стьюдента:
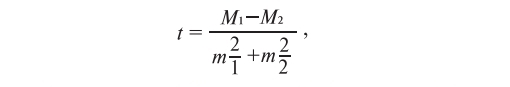
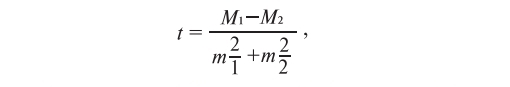
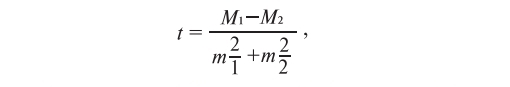
где M1 — средняя арифметическая 1-й сравниваемой группы, M 2 — средняя арифметическая 2-й сравниваемой группы, m1 — средняя ошибка первой средней арифметической, m2 — средняя ошибка второй средней арифметической.
Статистическая обработка результатов исследования в группах проводилась с определением значимости с помощью непараметрического U-критерия Манна—Уитни.
Формула U-критерия Манна—Уитни:
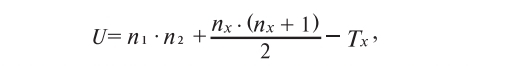
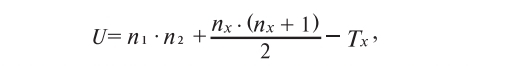
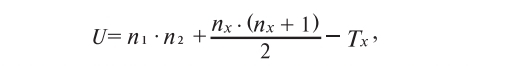
где n1 — количество элементов в 1-й выборке, n2 — количество элементов во 2-й выборке, Тх — большая из 2 ранговых сумм, nх — соответствующая выборка.
Показатели, изменяющиеся в динамике, анализировались с помощью парного критерия Стьюдента (в случае нормального распределения) или с использованием t-критерия Вилкоксона.
Для анализа качественных показателей использовался критерий χ2 c поправкой Йетса (в случаях абсолютных чисел менее 10), при невозможности его использования применялся Z-критерий для долей с поправкой для концевых точек. Статистически значимым различие между группами считалось при p<0,05.
На основании анализа изменений средней температуры тела в двух группах было выявлено, что в 1-й группе пациентов, которые рассасывали препарат Арника Монтана С9 (БУАРОН), температура в послеоперационном периоде нормализовывалась быстрее, максимально повышалась до 37,1 °С утром и 37,4 °С в вечернее время (рис. 2; рис. 3 на цв. вклейке). С помощью теста Манна—Уитни было показано, что день нормализации утренней температуры тела в 1-й группе наступал статистически значимо раньше, чем в контрольной группе (p-value=0,0002<0,05). Однако статистически значимой разницы в вечерней температуре те-ла между группами не наблюдалось.
Выраженность послеоперационной боли оценивалась по ВАШ (рис. 4 на цв. вклейке) утром в покое после пробуждения, а также при глотке воды. У пациентов 1-й группы болевой синдром стихал быстрее, чем у пациентов 2-й группы (рис. 5 на цв. вклейке).
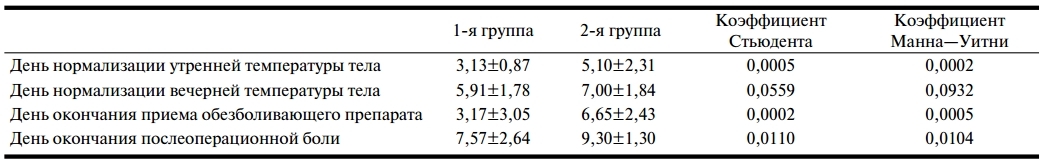


Пациенты обеих групп отмечали в анкете необходимость применения обезболивающих препаратов (инъекции препарата Кеторолак внутримышечно), а также часто-ту применения в течение всех 10 дней наблюдения. Пациенты 1-й группы требовали обезболивающие препараты в среднем меньше: в 1-е сутки после операции 60,9% пациентов 1-й группы и 85% пациентов 2-й группы. Пациенты, принимающие препарат Арника Монтана С9 (БУ-АРОН) максимально, использовали обезболивающие 3 раза в сутки с 1—6-х суток, а пациенты, не принимавшие препарат Арника Монтана С9 (БУАРОН), — 4—5 раз в сутки, что указывает на эффективность применения данного препарата в лечении болевого синдрома (рис. 6 на цв. вклейке). Стоит отметить, что в 1-й группе день окончания приема обезболивающего и день окончания после-операционной боли наступали статистически значимо раньше, чем в контрольной группе; в тесте Манна—Уитни значения p-value были равны 0,0005 и 0,0104 соответственно, что ниже установленного порога значимости 0,05 (см. таблицу).
При оценке фарингоскопической картины наблюдалась разница в выраженности отечности слизистой оболочки глотки в области послеоперационной раны. Отек слизистой оболочки небных дужек и мягкого неба характеризовали в баллах от 1 до 3. Где 0 баллов — отсутствие отека, 1 балл — отек слизистой оболочки небных дужек, 2 балла — отек мягкого неба, 3 балла — выраженный отек язычка мягкого неба (uvula). В первые сутки после операции у большинства пациентов в обеих группах наблюдался отек слизистой оболочки глотки в разной степени выраженности. На 4-е сутки в группе пациентов, получающих Арника Монтана С9 (БУАРОН), отек язычка мягкого неба не наблюдался ни у одного пациента. Однако в контрольной группе отек язычка мягкого неба на 4-е сутки был выявлен у 5% пациентов, перенесших тонзиллэктомию. На 10-е сутки после тонзиллэктомии незначительный отек небных дужек в 1-й группе отмечен только у 13% пациентов, против 55% пациентов в контрольной группе (рис. 7 на цв. вклейке).
В связи с возникающим послеоперационным воспалением в глотке у ряда пациентов наблюдалась лимфаденопатия шеи. В 1-й группе шейные лимфатические узлы увеличивались и становились болезненными всего у 34,8% пациентов, по сравнению с группой контроля, в которой лимфаденопатия шеи наблюдалась в 65% случаев (р=0,0480 критерий χ2). При этом лимфаденопатия шеи в 1-й группе преимущественно была только в 1-е сутки, к 4-м суткам от-мечена только у 1 (4,3%) пациента, в то время как в группе контроля к 4-м суткам лимфаденопатия шеи диагностировалась у 5 (25%) пациентов (возможно, из-за малочисленности выборки статистически значимых различий между группами не выявлено, однако можно отметить тенденцию к существенному сокращению лимфаденопатии шеи при использовании препарата Арника Монтана; р=0,0577).
На основании проведенного статистического анализа сравнения двух групп пациентов, которым была произведена двусторонняя тонзиллэктомия, у пациентов, получавших помимо обезболивающего препарата кеторолак, Арника Монтана С9 (БУАРОН) для рассасывания по 5 гранул 3 раза в день со 2-го дня, существенно сокращалось время выздоровления. На это указывают, в частности, более быстрое время нормализации температуры тела, исчезновение болей и уменьшение воспалительной реакции в глотке после тонзиллэктомии. Это может положительно влиять на качество жизни в раннем послеоперационном периоде пациентов, принимающих препарат Арника Монтана С9 (БУАРОН).
Авторы заявляют об отсутствии конфликта интересов.
Со списком литературы можно ознакомиться, скачав статью.






©Copyright 2026 Клиническая гомеопатия





